https://xn—–7kcdtvazpsfbrhe8b.khmelnitskiy.ua/
https://xn—-8sbebddid5cfnfjbfbboji9b.khmelnitskiy.ua/
https://xn——fddbdcb1be2adeglnjbebcbc2a4c8b.khmelnitskiy.ua/
https://мрт-хребта-спини.khmelnitskiy.ua
https://мрт-голови-головного-мозку.khmelnitskiy.ua
Нейрорадіологічні ознаки енцефалопатії у дітей з розладами спектрa аутизму, асоційованими з генетичним дефіцитом фолатного циклу
Одним із важливих досягнень у психіатрії та неврології останніх років є встановлення асоціації між генетичним дефіцитом фолатного циклу (ГДФЦ) і розладами спектрa аутизму (РАС) у дітей.
Докази такої асоціації ґрунтуються на результатах щонайменше п’яти метааналізів рандомізованих контрольованих клінічних досліджень і низки додаткових рандомізованих контрольованих випробувань, результати яких досі не систематизовані. Показано, що ГДФЦ призводить до розвитку низки типових біохімічних порушень, які зумовлюють особливу форму імунодефіциту і пов’язані з цим оксидативний стрес, котрий персистує, системне запалення, зокре- ма гіперпродукцію фактора некрозу пухлини-a (ФНП-a) та інших прозапальних цитокінів з нейро- токсичною дією, опортуністичні нейротропні інфекції, зокрема спричинені вірусами герпесу 6 (HHV-6) і 7 (HHV-7) типу, антимозкові автоімунні реакції до автоантигенів нейронів та мієліну. Видається очевидним, що ці три імунозалежні механізми церебрального пошкодження відіграють важливу роль у розвитку енцефалопатії при ГДФЦ, одним із клінічних виявів якої є РАС, однак загальну концепцію патогенезу хвороби досі належним чином не оформлено. Оскільки більшість вивчених шляхів ураження центральної нервової системи (ЦНС) при ГДФЦ мають імуноопосередкований характер, говорять про специфічне порушення нейроімунного інтерфейсу як модель формування енцефалопатії в таких випадках, що може бути використано при плануванні та проведенні клінічних досліджень у цьому напрямі.
Корисним для клінічної практики був би опис типових радіологічних ознак такої енцефалопатії, що поліпшило би виявлення хвороби та оптимізувало оцінку тяжкості стану пацієнта і ефективності лікувальних втручань. J. P. Hegarty та співавт. у спеціально спланованому клінічному дослідженні недавно показали, що радіологічні дані можуть бути потенційно інформативними для прогнозування результатів реабілітації дітей з РАС.
З огляду на багатокомпонентність патогенезу енцефалопатії при ГДФЦ, слід очікувати виявлення комплексу нейровізуалізаційних ознак, які теоретично мають корелювати з реалізацією певних механізмів церебрального пошкодження, які є причиною їх розвитку, і появою клінічних симптомів, котрі є наслідком їх виникнення.
Мета роботи – описати типові нейровізуалізаційні ознаки енцефалопатії у дітей з генетичним дефіцитом фолатного циклу і розладами спектрa аутизму та встановити кореляції між клінічними ознаками, механізмами пошкодження нервової системи і даними нейровізуалізації для оптимізації алгоритму діагностики, моніторингу та лікування.
Матеріали і методи
Ретроспективно проаналізовано медичні дані 225 дітей (183 хлопчики і 42 дівчинки) віком від 2 до 9 років з ГДФЦ та клінічними виявами за типом РАС. Усі вони були пацієнтами спеціалізованої нейроімунологічної клініки «Vivere» (реєстраційне досьє від 22.12.2018 № 10/2212-М). Отримання даних для дослідження та обробку матеріалу проведено згідно з договором № 150221 від 15.02.2021 р. та висновком комісії біоетичної експертизи (протокол № 140 від 21.12.2020 р. НМУ імені О. О. Богомольця).
Клінічний діагноз РАС установлено дитячими психіатрами за критеріями DSM-IV-TR (Diagnostic and Statistical Manual of Mental Disorders) та ICD-10 (The International Statistical Classification of Diseases and Related Health Problems).
Патогенні поліморфні варіанти генів фолатного циклу визначали методом полімеразної ланцюгової реакції (ПЛР) з рестрикцією на підставі виявлення заміни нуклеотидів MTHFR C677T у моно- формі (n = 68), а також у поєднанні з іншими замінами нуклеотидів – MTHFR A1298C, MTRR A66G і/або MTR A2756G (n = 157). Ці особи утворили досліджувану групу. До контрольної групи ввійшла 51 клінічно здорова дитина (37 хлопчиків та 14 дівчаток) аналогічного вікового розподілу, які не страждали на ГДФЦ.
Оцінювали тяжкість клінічних симптомів РАС за спеціалізованою шкалою Aberrant Behavior Checklist (АВС).
Лабораторне параклінічне обстеження дітей груп спостереження проводили з урахуванням сучасних уявлень щодо механізмів пошкодження ЦНС при РАС, асоційованих з ГДФЦ. Діагностику реактивованих герпесвірусних інфекцій здійсню- вали методом ПЛР лейкоцитів крові (відділ нейробіохімії Інституту нейрохірургії імені А. П. Ромоданова НАМН України) відповідно до даних дослідження G. L. Nicolson та співавт.
Виявлення b-гемолітичного стрептокока групи А проводили шляхом бактеріологічного посіву зі слизової ротоглотки на селективному поживному середовищі або за специфічним антитоксичним імунітетом у сироватці крові (антистрептолізин-О, антистрептодорназа, антигіалуронідаза) (ELISA; MDI Limbach Berlin GmbH, Німеччина). Додатково проводили визначення панелі Канінгем (Cunningham Panel™) з метою ідентифікації автоантитіл до нейронів підкіркових гангліїв (ELISA, cell-based assay; Moleculera Labs Inc, США). Оцінювали результати серологічних досліджень сироватки крові на предмет виявлення специфічних антинейрональних автоантитіл, які валідовані як маркери автоімунних лімбічних енцефалітів у дітей та дорослих, а саме автоантитіл до глутамінокисної декарбоксилази (GADA), калієвих каналів нейронів, амфіфізину, NMDA-рецепторів нейронів, GABA, СV2, Yo, Ro, Hu, AMPAR 1 і 2 (імуноферментний аналіз; MDI Limbach Berlin GmbH, Німеччина), що відповідає сучасним підходам до діагностики автоімунних лімбічних енцефалітів.
Сироваткову концентрацію ФНП-a вимірювали методом імуноферментного аналізу (норма < 8,1 пг/мл) («Сінево», Україна).
Нейровізуалізацію проводили за допомогою магнітно-резонансної томографії (МРТ) головного мозку у конвенційних режимах (Т1 і Т2-зважені, FLAIR) на томографах з величиною магнітної індукції котушки 1,5 Тл. Відео-електроенцефалографічний моніторинг здійснювали шляхом 30-хвилинногозапису біоелектричної активності кори головного мозку дитини у стандартних відведеннях з пробами фотостимуляції та гіпервентиляції.
Статистичну обробку матеріалу проводили шляхом порівняльного і структурного аналізу. Для ви- значення вірогідності відмінностей між показниками у групах спостереження використовували параметричний Т-критерій Стьюдента з показником довірчої ймовірності (р) та непараметричний критерій – число знаків Z за Ю. В. Урбахом. Вірогідними вважали відмінності при р < 0,05 і Z < Z0,05. Для вивчення асоціацій між досліджуваними показниками застосовували відношення шансів (ВШ) та 95 % довірчий інтервал (ДІ).
Для проведення статистичних розрахунків користувалися програмою Microsoft Excel.
Результати та обговорення
Аналіз МР-знімків у дітей з РАС, асоційованими з ГДФЦ, як і очікувалося, виявив низку нейровізуалізаційних ознак, які були типовими для цієї категорії пацієнтів і не спостерігалися у здорових осіб. Усі виявлені нейрорадіологічні ознаки можна об’єднати щонайменше в 5 різнорідних груп за їх характером. По-перше, відзначено вияви лейкоенцефалопатії різного ступеня тяжкості з переважним порушенням мієлінізації в білій речовині тім’яних часток півкуль великого мозку перивентрикулярно в так званих перитригональних зонах – ділянках термінальної мієлінізації (89 % випадків у досліджуваній групі та лише 17 % – у контрольній групі, р < 0,05, Z < Z0,05). Оскільки радіологічні вияви лейкоенцефалопатії спостерігали майже в усіх пацієнтів досліджуваної групи, можна вважати ці зміни класовою ознакою для дітей з РАС, асоційованими з ГДФЦ. По-друге, мали місце вияви скроневого медіанного склерозу (tempo- ral mesial sclerosis) з ураженням гіпокампів, парагіпокампальних звивин, мигдалеподібних тіл і острівців (67 % випадків у досліджуваній групі та лише 12 % – у контрольній групі, р < 0,05, Z < Z0,05). По-третє, виявлено симптоми гіпертрофії підкіркових гангліїв півкуль великого мозку, здебільшого – хвостатих ядер, з компресією передніх рогів бічних шлуночків (39 % випадків у досліджуваній групі та лише 7 % – у контрольній групі, р < 0,05, Z < Z0,05). По-четверте, діагностували нейрорадіологічні ознаки природженої СMV-нейроінфекції (відповід- но 7 та 2 % випадків, р < 0,05, Z < Z0,05) і залиш- кові явища постнатально перенесених вірусних енцефалітів (16 та 0 % випадків, р < 0,05, Z < Z0,05). По-п’яте, ідентифікували вияви так званих малих аномалій розвитку головного мозку (48 і 22 % ви- падків, р < 0,05, Z < Z0,05) (рис. 1).
Поєднання 4-5 груп нейрорадіологічних ознак енцефалопатії розглядали як повний нейровізуалізаційний фенотип хвороби, тоді як наявність 1-3 груп інструментальних ознак ураження головного мозку – як неповний. Повний фенотип відзна- чено щонайменше в 40 % випадків, а неповний – у 60 %. Повний нейрорадіологічний фенотип енцефалопатії був асоційований з тяжчим клінічним станом пацієнта за шкалою АВС порівняно з особою з неповним фенотипом (р < 0,05, Z < Z0,05).
Лейкоенцефалопатія, яка виявлялася на МР- знімках у вигляді плямисто або мозаїчно нерівномірно розподіленого гіперінтенсивного сигналу помірної або слабкої вираженості з нечіткими контурами в Т2-зваженому режимі та режимі FLAIR, відрізнялася за тяжкістю і поширеністю у пацієнтів досліджуваної групи (рис. 2, 3).
Можна було визначити дифузну форму лейкоенцефалопатії, за якої порушення мієлінізації були майже рівномірно розподілені між різними частками півкуль великого мозку (22 % випадків). Частіше відзначали вогнищеві форми ураження білої речовини півкуль, причому тім’яна частка залучалася найчастіше, особливо – в перивентрикулярній зоні, де, як відомо, дозрівання мієлі- ну протягом онтогенезу відбувається найпізніше. Лобно-скронево-тім’яні ураження білої речовини півкуль великого мозку мали місце в 13 % випадків, скронево-тім’яні – у 16 %, лобно-тім’яні – в 11 %, лобно-скроневі – в 3 %, ізольовані ураження білої речовини тім’яних часток – у 15 %. Спостерігали менш виражені радіологічні вияви лейкоенцефалопатії у дітей старшої вікової групи (> 4 років) порівняно з дітьми віком 2-4 роки (р < 0,05, Z < Z0,05), що, ймовірно, відображує процес затриманого дозрівання мієліну у дітей з РАС, асоційованими з ГДФЦ.
Про мієлінопатію у дітей з ГДФЦ повідомляли раніше. Зокрема T. Strunk та співавт. доповіли про феномен полегшеної демієлінізації в білій речовині півкуль великого мозку при ГДФЦ, описавши підгостру лейкоенцефалопатію у пацієнта з гетерозиготною патологічною поліморфною заміною нуклеотиду MTHFR C677T при застосуванні метотрексату в низькій терапевтичній дозі. L. M. Marseglia та співавт. у контрольованому клінічному дослідженні виявили зв’язок між наявністю генотипів MTHFR A1298C і A1298C/ C677T і появою патологічного гіперінтенсивного МР-сигналу в Т2-зваженому режимі та режимі FLAIR у ділянці білої речовини півкуль великого мозку у доношених новонароджених, а саме перивентрикулярної демієлінізації та втрати об’єму білої речовини навколо шлуночків з розвитком вікарної вентрикуломегалії. A. Y. Hardan та співавт. провели спеціально сплановане клінічне дослідження стану білої речовини півкуль великого мозку у дітей з РАС на підставі аналізу результатів МР-спектроскопії головного мозку ((1)H-MRS) з отриманням мультивоксельних ехо-часових in vivo (1)H-MRS-даних. Протонна МР-спектроскопія продемонструвала особливий патерн метаболіч- них порушень, зокрема аномальне зменшення величини співвідношення N-ацетиласпартат/креатин, що вказувало на велике багатовогнищеве нерівномірно розподілене пошкодження мієліну і аномальний розвиток аксонів у білій речовині півкуль великого мозку у дітей з РАС.
Скроневий медіанний склероз (рис. 4), який виявлявся на МР-знімках у вигляді гіперінтенсивного сигналу від основних структур мезолімбічної системи скроневих часток півкуль великого мозку в Т2-зваженому режимі та режимі FLAIR, у дітей досліджуваної групи, також відрізнявся за вираженістю та поширеністю патологічних нейро- візуалізаційних змін у різних пацієнтів. Тотальна форма ураження із залученням усіх чотирьох осно- вних структур мезолімбічної системи мала місце в 43 % випадків, а парціальні форми з ураженням 1-3 зазначених структур – у 57 %. Білатеральні ураження (76 % спостережень) переважали над унілатеральними (34 %). При парціальних уражен- нях структур мезолімбічної системи найчастіше спостерігали залучення гіпокампів (64 % випад- ків), рідше мав місце гіперінтенсивний МР-сигнал від острівців (53 %), парагіпокампальних звивин (47 %) та мигдалеподібних тіл (36 %). Ознаки атрофії структур мезолімбічної системи зареєстровано
у більшості пацієнтів досліджуваної групи (76 %), причому вияви атрофії та поширеність гіперінтен- сивного сигналу були більшими у пацієнтів стар- шої вікової групи (> 4 років) порівняно з дітьми віком 2-4 роки (р < 0,05, Z < Z0,05), що, ймовірно, відображує повільне прогресування скроневого медіанного склерозу у дітей з РАС, асоційовани- ми з ГДФЦ. В останніх частіше реєстрували при проведенні електроенцефалографії (ЕЕГ) епілеп- тиформну біоелектричну активність, переважно – у лобно-скроневих відведеннях (р < 0,05, Z < Z0,05), характерну для скроневої медіанної епілепсії, асоційованої зі скроневим медіанним склерозом (mesial temporal lobe epilepsy associated with hip- pocampal sclerosis, MTLE-HS).
Отримані нами дані узгоджуються з результа- тами спеціально спланованого ретроспективного клінічного дослідження L. Monge-Galindo та співавт. Автори висвітлили досвід діагностики скроневого медіанного склерозу в одному клінічному центрі протягом останніх 19 років у дітей із симптомами порушеного розвитку. Причинами зазначеного церебрального ураження були герпесвірусна інфекція, цитомегаловірус, пренатальна церебральна патологія. У 5 пацієнтів мав місце ізольований епілептичний синдром, у 1 – затримка психомоторного та інтелектуального розвитку, ще в 1 – РАС, у 3 – епілептичний синдром із затримкою психомовленнєвого розвитку, ще у 1 – РАС з епілептичним синдромом, у 2 – РАС із затримкою психомовленнєвого розвитку, ще у 2 – РАС з епілептичним синдромом і затримкою пси- хомовленнєвого розвитку, в 1 – тяжкі мігренозні цефалгічні пароксизми.
Гіпертрофія підкіркових гангліїв півкуль великого мозку здебільшого мала білатеральний і майжесиметричний характер (67 % випадків; рис. 5). Унілатеральні ураження зареєстровано в 33 % випадків. Переважно залучалися хвостаті ядра (89 % випадків) як ізольований радіологічний синдром або в по-єднанні з ураженням інших підкіркових ганглїів (шкаралупи, блідого і сочевицеподібного ядер; 27 % випадків). Повна компресія передніх рогів бічних шлуночків унаслідок збільшення розмірів хвостатих ядер мала місце в 47 % випадків, часткова – в 53 %. Не виявлено відмінностей за нейровізуалізаційними виявами гіпертрофії підкіркових вузлів між пацієнтами різних вікових груп (р > 0,05, Z > Z0,05).
Результати ЕЕГ, отримані у цієї категорії пацієнтів, вкладаються у три патерни патологічних порушень біоелектричної активності кори головного мозку. В разі початкових МР-ознак гіпертрофії хвостатих підкіркових гангліїв відзначали вияви локального гіперзбудження біоелектричної активності в проекції підкіркових вузлів півкуль великого мозку (рис. 6). У пацієнтів з виявами вираженішого збільшення розмірів nn. caudati реєстрували ознаки білатеральних латералізованих синхронних електричних розрядів (рис. 7). У разі МР-ознак тяжкої гіпертрофії хвостатих підкіркових ядер з повною компресією передніх рогів бічних шлуночків мала місце дифузна гіперсинхронізація біоелектричних кіркових ритмів (рис. 8).
Про гіпертрофію підкіркових гангліїв як радіологічний біомаркер говорять у контексті субкортикальних автоімунних енцефалітів у дітей і дорослих (PANS/PITANDS/PANDAS; pediatric acute-onset neu-ropsychiatric syndrome/pediatric infection-triggered autoimmune neuropsychiatric disorder/pediatric autoimmune neuropsychiatric disorders associated with streptococcal infections). Раніше повідомляли, що у дітей з РАС, асоційованими з ГДФЦ, щонайменше в третині випадків відзначають клініко-радіологічні ознаки субкортикального автоімунного енцефаліту, що може пояснити отримані нейровізу алізаційні дані у дітей досліджуваної групи.
Під нейровізуалізаційними ознаками перене- сеної природженої СMV-нейроінфекції розуміли пентаду інструментальних симптомів: вентрикуло- мегалію, гіпоплазію мозолистого тіла, симетричні кісти в полюсах скроневих часток, великі поля демієлінізації в білій речовині півкуль великого моз- ку та перивентрикулярні кальцинати (рис. 9, 10). Повний нейрорадіологічний фенотип зареєстровано в 79 % випадків, частковий (3-4 ознаки) – в 21 %. Мали місце лише білатеральні та лише асиметричні ураження. Ці зміни зазвичай поєдну- валися з ознаками васкулопатії стріарних артерій, які виявляли при нейросонографічному дослідженні в антенатальний період і/або протягом першого року після народження.
Магнітно-резонансна томографія в діагностиці гострого інсульту
Вступ
Загальні дані
Магнітно-резонансну томографію (МРТ) все частіше застосовують в діагностиці гострого ішемічного інсульту (ОІІ). Мета цієї статті – простим і доступним чином викласти сучасні дані про застосування МРТ в діагностиці ОІІ. МРТ – метод візуалізації, який швидко розвивається і дозволяє з досить високою специфічністю виявляти зміни, пов’язані з інсультом. Звичайно, він має і недоліки, такі як висока вартість, тривалість проведення дослідження і більш низька чутливість до субарахноїдальним крововиливом. Недавні досягнення, такі як підвищена потужність магнітного поля (1,5-3 Т), нові послідовності візуалізації і апарати з відкритим контуром для пацієнтів з клаустрофобію і ожирінням сприяють ще більшому поширенню методики в діагностиці ОІІ.
Патологічна фізіологія
При попаданні в сильне магнітне поле деякі ядра атомів тіла людини переходять в збуджений стан; вони адсорбують радіочастотну енергію магнітного поля і потім віддають її при повній релаксації. Енергія вивільняється з збудженої тканини протягом короткого періоду часу відповідно до однієї з двох констант релаксації – Т1 і Т2 послідовностей, а яку випромінює енергія конвертується в зображення. Контрастність останніх обумовлена різною інтенсивністю випромінюваних сигналів, яка в свою чергу пов’язана з різною концентрацією ядер в тканинах організму.Водень (протони) – один з найбільш поширених атомів в тканинах людського організму. Застосовувалися й інші органічні субстанції, але вони дозволяють отримати меншу просторову роздільну здатність. Вивчаються біохімічні склади, такі як лактат і N-ацетил аспартат, з тим, щоб зрозуміти значущість різних концентрацій цих компонентів при різних патологічних станах (магнітно-резонансна спектроскопія (МРС)).Найбільш часто вживані види МР-візуалізації такі:
- Т1-зважені зображення (Т1ВІ), на яких ліквор (цереброспінальної рідина) має низьку інтенсивність сигналу в порівнянні з мозковою тканиною;
- Т2-зважені зображення (Т2ВІ), на яких ліквор має більш інтенсивний сигнал в порівнянні з мозковою тканиною;
- зображення, зважені по спінової щільності, при яких ліквор має однакову щільність з мозком;
- послідовності градієнтного відлуння, які дозволяють з високою чутливістю виявляти ранні геморагічні зміни;
- дифузно-зважена візуалізація (ДВВ), при якій на зображеннях видно випадкові мікроскопічні руху молекул води;
- перфузійному-зважені зображення (ПВІ), на яких гемодинамически зважені МР-послідовності грунтуються на проходженні контрасту через мозкову тканину.
Патогенез формування знахідок, виявлених при візуалізації
Незалежно від причини ішемія нейронів призводить до виснаження внутрішньоклітинних запасів аденозинтрифосфорної кислоти (АТФ), в результаті чого порушується робота пов’язаних з мембраною АТФ-залежних іонних каналів, які відповідальні як за підтримку мембранних потенціалів спокою, так і за генерацію потенціалів дії. Ці мембранні аберації призводять до накопичення іонів всередині клітини (включаючи кальцій), і таким чином створюється градієнт, що обумовлює накопичення води і розвиток цитотоксического набряку клітини.Мозкові ендотеліальні клітини мають більш високу резистентність до ішемії, ніж нейрони і глия. Приблизно через 3-4 годин після розвитку ішемії цілісність гематоенцефалічного бар’єру порушується і протеїни плазми крові починають потрапляти в позаклітинний простір. Потім, після реперфузії, за ними слід вода, що призводить до розвитку вазогенного набряку; цей процес починається через 6 годин після інсульту і досягає максимуму на 2-4-й день. Реперфузія також може супроводжуватися геморагічної трансформацією вогнища інфарцірованія, що найчастіше буває при великих кортикальних інфарктах.Зміни на МР-зображеннях, пов’язані з ОІІ, розташовуються в зоні кровопостачання закупорити судини, що в цілому типово для цереброваскулярної патології і корисно при диференціальної діагностики.
Летальність і інвалідизація
Застосування клінічних даних та даних МРТ для прогнозування результатів ОІІ
ДВІ дозволяє оцінити ядро інфаркту, а ПВІ – ішемічну півтінь ( «пенумбра»). Невідповідності цих зображень і є та тканину, яка потенційно залишиться живий після реперфузії. Але, незважаючи на дані на користь «гіпотези невідповідності», немає переконливих даних про те, що лише тільки наявність такої невідповідності дозволяє виявити пацієнтів, які дадуть відповідь на терапію. Недостатня стандартизація може бути однією з проблем.RRE-90 – проста прогностична шкала, в якій враховуються клінічні і візуалізаційні дані, що дозволяють оцінити ранній ризик розвитку повторного інсульту в гострий період ОІІ (табл. 1). Було показано, що RRE-90 має гарну предиктивної силою, і якщо зовнішні дослідження верифікують ці дані, то її можна буде застосовувати для створення індивідуалізованих алгоритмів лікування пацієнтів (табл. 2).

рентгенографія
З метою виявлення металевих імплантатів і чужорідних тіл (водії ритму, судинні кліпси, штучні серцеві клапани і ін.) Іноді проводять звичайну рентгенографію.
методики МРТ
Дифузно-зважена візуалізація
ДВВ чутлива до мікроскопічних випадковим рухам протонів води – коефіцієнт дифузії (ADC, від англ. Apparent diffusion coefficient), який як раз і визначається за допомогою цього методу візуалізації. Молекули води рухаються у напрямку градієнта магнітного поля; вони накопичують фазовий зсув, який має пряме відношення до ослаблення зображення.У численних дослідженнях було показано, що ADC ішемічних зон на 50% і більше менше, ніж аналогічні показники нормальних зон мозку. На дифузно-зважених зображеннях (ДВІ) вони виглядають як яскраві (гіперінтенсивні) ділянки (рис. 1). Показано, що зміни ADC відбуваються вже через 10 хв після розвитку ішемії.
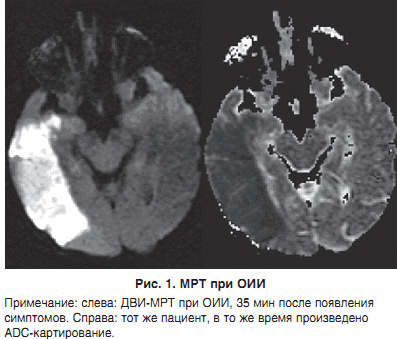
Цитотоксичний набряк розвивається внаслідок порушення функції калій-натрієвих насосів, яке в свою чергу є наслідком метаболічних порушень, пов’язаних з ОІІ; це відбувається протягом декількох хвилин після розвитку ішемії і призводить до підвищення обсягу води в церебральної тканини на 3-5%. Передбачається, що зниження інтенсивності руху молекул води між поза- і внутрішньоклітинним простором є причиною зниження показника ADC.Дифузія молекул води регулюється біологічними бар’єрами (наприклад клітинними мембранами і органеллами). Поведінка молекул води несиметрично і при вимірюванні ADC в одному напрямку розподіл може бути нерівним; це може створювати неправильне уявлення про патологічному вогнищі. Показник ADC вимірюють в кількох напрямках (3, 6 або більше), а картування його виробляють з тим, щоб отримати незалежні від напрямку дані про дифузії. При вимірі ADC в 6 або більше напрямках можна розрахувати рух всіх молекул води ( «тензорна матриця») – повне дифузне тензорне картування, яке можна застосовувати для візуалізації шляхів білої речовини.Зниження ADC може відзначатися при інших станах, таких як глобальна ішемія, гіпоглікемія і епілептичний статус; тому слід брати до уваги клінічний стан пацієнта.У дослідженнях, проведеному у людей, було показано, що пошкодження в зонах зі зниженим ADC дуже рідко оборотні, хоча в декількох дослідженнях повідомлялося, що інтраартеріальний тромболізис іноді призводить до регресу дифузійних дефектів. Методикою, яку найчастіше застосовують для отримання ДВІ, є ультрашвидкий ехопланарная візуалізація (ЕПШ); вона дозволяє значно зменшити тривалість сканування і нівелює рухові артефакти.Різке зниження показника ADC поступово приходить в норму на 5-10-й день після розвитку ішемії (псевдонормалізація); згодом він навіть перевищує нормальні значення, що іноді дозволяє відрізняти гострі, підгострі і хронічні вогнища.ДВІ має дуже високу чутливість і відносної специфічністю у виявленні ОІІ; проте в недавніх дослідженнях було показано, що дрібні лакунарні інфаркти можуть бути втрачені. Нормальні результати ДВ-МРТ у пацієнта З ІНСУЛЬТОПОДІБНИМ симптомами повинні направляти лікаря на пошук інших неішемічної причин симптомів. Аномалії дифузії відзначаються практично у 50% пацієнтів, які перенесли ТІА.На підставі клінічного досвіду співробітників інсультного центру Chapel Hill Університету Північної Кароліни, диференціація гіперінтенсивного зон при ДВІ виглядає наступним чином:
- підгострий ішемічний інсульт – гіперінтенсивного регресує через 7-14 днів;
- геморагічний інсульт – зазвичай світлий на Т1ВІ;
- бляшки при розсіяному склерозі – також світлі на FLAIR-зображеннях і Т2ВІ;
- травма голови – травма в анамнезі;
- абсцес головного мозку – посилення вогнища у вигляді кільця при візуалізації з контрастом;
- судинні сплетення – зазвичай розташовуються всередині шлуночків, можуть бути двосторонніми;
- епідермоід – зазвичай локалізується екстрааксіально;
- повітря в кістки – зазвичай з двох сторін, в скроневої кістки.
Перфузійному-зважена візуалізація
Ця методика дозволяє отримати дані про перфузії головного мозку. Найбільш часто вживаним методом є болюс-контрастний трекінг, при якому візуалізація ґрунтується на моніторингу недіффундірующего контрастної речовини (гадоліній), що проходить через мозкову тканину.У міру проходження контрасту через зону інфарцірованія інтенсивність сигналу знижується і потім стає нормальною в міру переходу до здорової тканини. Крива, отримана на підставі цих даних ( «крива розмитості сигналу» від англ. Signal washout curve), відображає і дозволяє оцінити обсяг крові в мозку (ОКМ, син. «Церебральний об’єм крові»).Функцію артеріального припливу можна виміряти на нижніх зрізах або за допомогою вимірювання концентрації гадолінію, яка пропорційна змінам на Т2ВІ при введенні контрасту в низьких дозах (<3 мг / кг). На підставі цих даних можна отримати кількісні карти мозкового кровотоку (МК), ОКМ, середнього часу транзиту (СВТ) і часу до пікових показників (ВДП), а також багато інших гемодинамічні параметри. Ведуться дискусії про те, які параметри ПВІ необхідно використовувати. У більшості центрів США застосовують такі показники, як СВТ і ВДП.Було показано, що ДВІ і ПВІ – більш ефективні методи діагностики ОІІ, ніж рутинна МРТ, як в гострій фазі захворювання, так і протягом 48 годин після події. Дуже важливо застосовувати обидві ці техніки, так як разом вони дозволяють отримати інформацію про локалізацію і поширеність зони інфарцірованія вже в перші хвилини після розвитку інсульту; при повторному проведенні методики дозволяють відслідковувати розвиток ішемічного вогнища. Ці дані можуть мати велике значення при виборі методу лікування, а також в прогнозуванні результатів захворювання.Протягом декількох днів на повторних ДВІ вогнище зазвичай збільшується. Передбачалося, що цей процес можна зупинити, якщо рано провести реперфузію. Невеликі осередки на ПВІ зазвичай не збільшуються.Дифузійно-перфузионное невідповідність зазвичай являє собою ішемічну півтінь – зону неповної ішемії, яка лежить безпосередньо біля ядра зони інфарцірованія. Пенумбра розглядають як життєздатну область, яка, однак, знаходиться під загрозою ішемії; її можна врятувати, якщо швидко провести необхідні втручання. Життєздатність цієї зони зберігається до 48 год після розвитку ОІІ. Визначення обсягу ішемічної півтіні може бути корисним при відборі пацієнтів для проведення тромболітичної терапії і можливо навіть для таких рутинних методів, як каротидної ендартеректомія та підвищення артеріального тиску. Це також може бути корисно в визначенні співвідношення ризик / користь від застосування цих методів лікування (рис. 2).
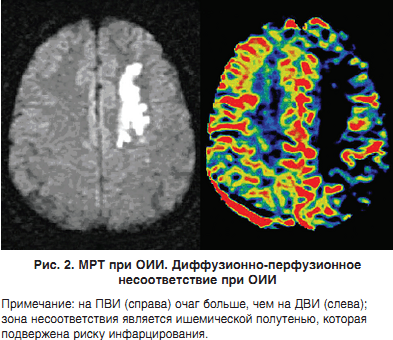
Недоліки показника диффузионно-перфузійного невідповідності в основному методологічні та включають: (1) недостатнє анатомічне відповідність ПВІ і ДВІ; (2) різну чутливість ПВІ в залежності від затримки Тmax; (3) візуальну оцінку невідповідності.МРТ досі має деякі обмеження до застосування, зокрема у пацієнтів з металевими імплантатами та у пацієнтів в критичному стані, яким необхідний постійний моніторинг.Ці нові методи – ДВІ і ПВІ – є найбільш перспективними галузями застосування МРТ щодо їх можливостей виявляти ранні зміни (перші хвилини після інсульту). В даний час їх застосовують в клінічних дослідженнях для оцінки ефективності тромболітичної і нейропротектівний терапії у пацієнтів з ОІІ.
МРТ, залежне від концентрації кисню крові (BOLD – blood oxygen level-dependent)
Фракція екстракції кисню (ФЕК), яку визначають за допомогою позитронно-емісійної томографії, вважається стандартом візуалізації ішемічної півтіні при ОІІ. До сих пір МР-ДВ / ПВ-візуалізація є єдиною МР-методикою, яка дозволяє оцінити зону оборотного пошкодження мозку.BOLD є новим методом, який дозволяє визначати деоксігемоглобін в церебральних капілярах і венах як МР-індикатор церебральної ФЕК. За даними недавніх досліджень, BOLD-МРТ дозволяє більш ефективно оцінити ішемічну півтінь при ОІІ, ніж показник МР-ПВ / ДВ-невідповідності. Для розуміння клінічного значення цього методу візуалізації потрібні подальші дослідження.
Ехопланарная візуалізація
ЕПШ є новим методом, який можна застосовувати для візуалізації фізіологічних процесів і оцінки коефіцієнтів дифузії ишемизированного мозку. Зміни церебральної оксигенації можна проводити моніторинг за допомогою послідовностей градиентного луни і ЕПШ, на яких деоксігенірованная кров поводиться як контрастну речовину.ЕПШ можна застосовувати в поєднанні з введенням контрастної речовини з метою оцінки церебральної перфузії і функціональних змін ОКМ.При використанні цього варіанту візуалізації зони гіпоперфузії після ін’єкції контрастної речовини виглядають гіперінтенсивного. Ця методика менш витратна за часом.
Магнітно-резонансна спектроскопія
МРС є одним з недавніх технологічних досягнень в області МР-технологій; метод дозволяє оцінити метаболічну активність і концентрації деяких метаболітів в специфічних областях мозку. Проводилися спектроскопічні дослідження із застосуванням протонів і фосфору.МРС дозволяє виявити зниження вмісту N-ацетил аспартату, який вважається маркером нейронів і є найбільш частим ознакою при гострому інсульті. Цей стан може розвинутися протягом декількох годин після розвитку інсульту і потім продовжуватися в підгострій і хронічній фазах інсульту, ймовірно, через втрату нейронів. Підвищення вмісту лактату – ще одна важлива ознака, який пояснюють анаеробним метаболізмом ішемізованої тканини. Дослідження інших метаболітів, таких як холін і креатин, показали зниження їх рівня при ОІІ.Фосфорна спектроскопія дозволяє отримати інформацію про енергетичну метаболізмі і pH, виснаженні запасів АТФ, зниженні тканинного pH і підвищенні співвідношення неорганічних фосфатів та фосфокреатину; це було показано як в клінічних, так і в експериментальних дослідженнях.Велика тривалість дослідження, слабкість сигналу і низьке просторову роздільну здатність є основними обмеженнями застосування МРС в клінічній практиці для оцінки церебральної ішемії; проте в ряді публікацій повідомляється, що результати МРС можуть мати при ОІІ прогностичне значення.
Магнітно-резонансна ангіографія
Магнітно-резонансна ангіографія (МРА) дуже чутлива до потоку і грунтується на відмінностях сигналу між рухомою кров’ю і нерухомою тканиною мозку; в результаті можна отримати ангіограммоподобние зображення судин шиї та голови.Метод МРА важливий в діагностиці розшарувань, причому на зображенні можна побачити як помилковий, так і справжній просвіт ураженої судини. Далі буде наведено короткий опис двох основних методик.Тривимірна часопролітної методика (від англ. 3D time-of-flight, 3D-TOF) ґрунтується на посиленні, пов’язаному з потоком; це кращий метод. Тим не менш, він має деякі недоліки, одним з яких є втрата сигналу від турбулентного потоку крові в звивистих і стенотично сегментах судин, що ускладнює оцінку стенозу в цих областях. Останні є найбільш частими вогнищами локалізації атеросклеротичних уражень. Крім того, в зонах з повільним кровотоком спінова насиченість сканів призводить до переоцінки стенозу. При проведенні дослідження з контрастуванням можна отримати більше інформації, ніж при стандартній ангіографії, особливо у виявленні критичних стенозів позачерепних судин, але метод менш надійний в діагностиці інтракраніальних критичних стенозів. Завжди треба пам’ятати про те,Двомірна TOF-МРА (2D-TOF) також грунтується на відносній контрастності між поточною кров’ю і нерухомою тканиною. Метод дозволяє отримати більш якісні зображення, ніж 3D-TOF МРА, в зонах з низькою швидкістю кровотоку. 2D-TOF-зображення при візуалізації патологічних змін зони біфуркації сонних артерій добре корелюють з даними каротидної ангіографії. Однак недоліками методики є часто відзначаються значні артефакти, які ускладнюють оцінку деталей, і тривалий час сканування.Модифікована TOF-МРА-методика, в якій застосовують множинне накладення тонких зрізів (multiple overlapping thin slab acquisitions – MOTSA), поєднує в собі переваги 2D і 3D TOF МРА. Метод виключно інформативний при візуалізації важкого стенозу, однак ступінь стенозу може кілька переоцениваться.Двомірна фазово-контрастна МРА є методикою, яка корисна при специфічної диференціації повільного кровотоку і його відсутності і нормального струму крові; вона захоплює лише тільки дійсно діючі судини. Для того, щоб не упустити деякі патологічні зміни, наприклад паравазального гематоми (які невізуалізіруются цим методом), поряд з фазово-контрастної МРА слід застосовувати інші послідовності візуалізації, такі як спіновий або градиентное відлуння. Ще одним недоліком фазово-контрастної МРА є втрата сигналу при турбулентному потоці в звивистих судинах.
типи інфарктів
тромбоемболічний інфаркт
Є найбільш частим варіантом. Зазвичай на МРТ вогнище виглядає клинообразно, розташовуючись в зоні кровопостачання будь-якої артерії. Недавні дані підтримують гіпотезу про те, що одиничний інфаркт в будь-якій зоні кровопостачання швидше тромботический, а множинні – скоріш за емболіческіе.
Інфаркти в «вододільних» зонах (в суміжних зонах кровопостачання)
Цей варіант розвивається в дистальних відділах зон кровопостачання окремих артерій. Він може розташовуватися як поверхнево, так і глибоко в мозковій паренхімі. Типові причини такого варіанту інсульту включають гіпотензію, зупинку серцевої діяльності і дихання, проксимальний стеноз артерії або її оклюзію. На МРТ при цьому відзначається неповний тромбоемболічний ішемічний інфаркт і раннє посилення паренхіми, що говорить про розвиток ранньої реперфузії. Відповідно до нових даних, цей тип інфаркту більш ефективно можна візуалізувати за допомогою ДВІ.
лакунарний інфаркт
Вважають, що ці маленькі глибокі церебральні інфаркти виникають через ураження дрібних судин, обумовленого ліпогіалінозом і фібриноїдним некрозом; їх найчастіше відзначають в осіб з гіпертензією або на цукровий діабет. Вогнища зазвичай локалізуються в базальних ядрах, внутрішньої капсулі, таламусі, стовбурі мозку і мозочку. Патерн візуалізації цих патологічних утворень аналогічний такому при тромбоемболічних інфарктах.
Венозний тромбоз і інфаркт
Оклюзія церебральних вен і венозних синусів зазвичай обумовлена системними станами, такими як вагітність, захворювання сполучної тканини, запальні ураження кишечника і стани, що супроводжуються гіперкоагуляції, але також і місцевими – інфекції, пухлини і травми. Оклюзія венозних структур обумовлює порушення відтоку аж до блокування кровотоку, що в результаті призводить до формування паренхіматозних інфарктів і геморагій. Пацієнтів зазвичай госпіталізують в кінці гострої фази або в підгострій фазі, що ускладнює діагностику, так як встановлення діагнозу в цих випадках залежить від методів візуалізації.Дані МРТ при цих варіантах інсульту включають відсутність сигналу від венозного струму крові, відсутність нормального венозного посилення і виявлення з- або гіперінтенсивного сигналів від венозних структур як в Т1-, так і в Т2ВІ. Ці варіабельні патерни посилення обумовлені різними продуктами крові, які містяться в патологічному вогнищі. Зміни зазвичай двосторонні, вони не відповідають зонам артеріального кровопостачання і часто поєднуються з крововиливами. Тривимірна фазово-контрастна МР-венографія є кращою методикою діагностики і оцінки венозних тромбозів.
Дані МРТ при гострому інсульті
Надгостре період (0-24 год)
МРТ-ДВВ дозволяє виявляти ішемічні зміни через кілька хвилин після їх розвитку. Знижений рух протонів знаходить своє відображення в зниженні показника ADC.На ранніх етапах церебральної ішемії ДВІ із застосуванням контрастування (перший пасаж введеного внутрішньовенно болюсно контрастної речовини) або спінових міток протонів води крові дозволяє виявити зниження мозкового кровотоку і хвилинний об’єм крові (МОК) і підвищення СВТ крові в мозку (рис. 3).
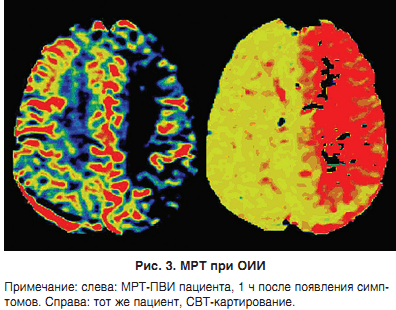
Зона накладення патологічних змін, виявлених при ДВ і ПВ-МРТ, корелює з областю інфарцірованія, в якій сталася необоротна загибель нейронів. Зона невідповідності (зміни в ПВ-режимі більше, ніж в ДВ), як уже говорилося, може бути ішемічної півтіні.Популярним останнім часом підходом є проведення МРТ для виявлення ДВ / ПВ невідповідності з метою відбору кандидатів для проведення лікування поза 3-годинного часового вікна. У двох недавно проведених клінічних дослідженнях ця гіпотеза піддавалася перевірці. У дослідженні DIAS-2 пацієнтам з більш ніж 20% невідповідністю ДВ / ПВ, за даними МРТ, проведеної протягом 3-9 годин після подій, випадковим чином призначали плацебо або десметеплазу. Аналогічним чином було побудовано дослідження EPITHET, але в ньому тимчасове вікно становило 3-6 ч. В обох дослідженнях не вдалося довести, що тромболізис, проведений після 3-годинного терапевтичного вікна, ефективний у пацієнтів з ДВ / ПВ-невідповідністю. У дослідженні ECASS-3 подібний підхід із застосуванням МРТ для відбору пацієнтів не використовувався,EPITHET і DIAS-2 підняли ряд питань технічного властивості, зокрема щодо (1) найбільш адекватного показника співвідношення ДВ / ПВ, (2) адекватного порога ПВ-МРТ, (3) одночасного проведення ДВ- і ПВ-МРТ і (4) автоматичної оцінки невідповідності.Для оцінки зони оборотної ішемії розробляються нові методики МРТ. Одним з таких методів є функціональна BOLD-МРТ.Через кілька годин після розвитку інсульту іноді спостерігається ефект втрати сигналу від судин (30-40% пацієнтів); це найкраще виявляється на T2ВІ.• Через 2-4 ч на Т1ВІ відзначається слабко згладжування борозен внаслідок цитотоксичної набряку.• Через 8 год на Т2ВІ виявляється гіперінтенсівний сигнал як наслідок цитотоксичної і вазогенного набряку.• Через 16-24 год на Т1ВІ відзначається гіпоінтенсівний сигнал внаслідок розвитку як цитотоксического, так і вазогенного набряку.На томограмах з контрастом виявляють артеріальний посилення, за яким слід паренхіматозне. Артеріальний посилення може бути дуже раннім (більш ніж у 50% пацієнтів), і воно обумовлено повільним кровотоком; зазвичай регресує через тиждень.Паренхиматозное посилення відрізняється при повних і неповних інфарктах. При повному інфаркті воно починається на 5-7-й день після інсульту і зберігається протягом декількох місяців. При неповних інфарктах воно може спостерігатися протягом 2-4 ч і зазвичай є більш інтенсивним, ніж при повних інфарктах.Хоча при використанні рутинних МР-послідовностей інсульт в гострій фазі побачити зазвичай не вдається, конвенціональна МРТ дозволяє виявити ознаки внутрішньосудинного тромбозу, такі як відсутність ефекту потоку (ефект «flow void») на Т2ВІ, гіперінтенсівний судинний сигнал в FLAIR-режимі і гіпоінтенсівний судинний сигнал в послідовності градієнтного відлуння (табл. 3).
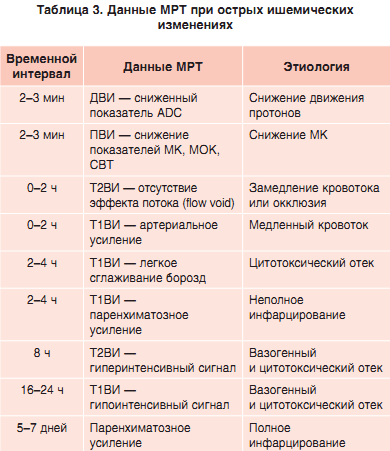
Гостра фаза (1-7 днів)
У цій фазі збільшується набряк, що досягає свого максимального розвитку через 48-72 год, і МР-сигнали стають більш явними і добре відмежовані. Ця ішемічна зона виглядає гіпоінтенсівно на Т1ВІ і гіперінтенсивного на Т2ВІ. У цій фазі можна оцінити мас-ефект.При дослідженні з контрастом артеріальний посилення зазвичай зберігається протягом всієї гострої фази, а паренхіматозне зазвичай оцінюють в кінці цієї фази (при повних інфарктах). При неповних інфарктах паренхіматозне посилення зазвичай відзначається раніше.Під час цього періоду, як правило, розвивається реперфузия і можуть розвиватися петехіальні і більші крововиливи, зазвичай через 24-48 год після розвитку інсульту. Зазвичай петехіальні геморагії є причиною розвитку феномена “затуманення” (fogging phenomenon), що безпосередньо обумовлено продуктами деградації гемоглобіну і маскує інфаркт як на Т1-, так і на Т2ВІ.
Подострая фаза (7-21-й день)
У цій фазі дозволяється набряк і мас-ефект стає менш вираженим; проте інфарцірованного області все ж виглядають гіпоінтенсівно на Т1ВІ і гіперінтенсивного на Т2ВІ. При дослідженні з контрастом артеріальний посилення до цього часу зазвичай регресує, а паренхіматозне ще зберігається протягом всієї фази.
Хронічна фаза (більше 21 дня)
У цій фазі повністю регресує набряк, а інфарцірованного зона все ще виглядає як гіпоінтенсівний вогнище в Т1ВІ і гіперінтенсівний в Т2ВІ. Через загибель тканини в зоні інфаркту відзначається ex vacuo шлуночків, розширення коркових борозен і звивин. На контрастних томограммах паренхіматозне посилення ще зберігається; воно зазвичай проходить через 3-4 міс.
МРТ при ТІА
У 1/3 до половини пацієнтів з ТІА відзначаються патологічні зміни на ДВІ. У багатьох цих випадках відповідні зони на Т2ВІ не виявляються. ПВІ, можливо, є більш чутливим методом, проте він адекватним чином не вивчалось у пацієнтів з ТІА. Характерно, що при виявленні патології на ДВ-МРТ у пацієнтів з ТІА не завжди відзначається инфарцирование на МРТ, проведеної згодом.Хоча ТІА традиційно розглядають як тимчасовий (триває менше 24 годин) неврологічний дефіцит судинного походження, застосування МРТ призвело до переосмислення цього визначення. Чи варто розглядати ДВІ-позитивні випадки ТІА як інсульт, залишається неясним.
МРТ при геморагічному інсульті
Послідовності градієнтного відлуння і ЕПШ дозволяють виявляти клінічно певні мікрокрововиливи, які не видно на рутинних МР і комп’ютерних томограмах. Ці мікрокрововиливи відзначаються у 1 / 5-1 / 4 пацієнтів з ішемічним інсультом і у 5% асимптомних індивідів похилого віку. Мікрогеморагії відображають наявність відкладень гемосидерину, а їх Гістопатологічні корелятом є що відбулася раніше екстравазація крові. Вони можуть бути проявами геморагічної ангиопатии і вказувати на підвищену імовірність розвитку геморагічної трансформації на тлі антикоагулянтної, антитромботичної і тромболітичної терапії.Послідовності градієнтного відлуння, ЕПШ і ДВІ чутливі до паренхіматозним геморрагиям (первинне внутрішньомозковий крововилив і геморагічна трансформація) в надгострій фазі (перші кілька годин), в той час як рутинне МРТ в Т1-і Т2ВІ-режимах дозволяє виявляти крововиливу в підгострій і хронічній фазах. Послідовність FLAIR може виявитися корисною в діагностиці екстрааксіальних скупчень крові (субдуральна гематоми). Відповідно до вищевикладеного, в сучасних клінічних посібниках не рекомендується замінювати комп’ютерну томографію МРТ для відбору пацієнтів для проведення тромболізису.
ускладнення
Різні ускладнення можуть розвиватися у пацієнтів, у яких є металеві імплантати (перегрів, дисфункція водія ритму і т.п.). Тому необхідно пам’ятати про це і уточнювати МР-сумісність імплантатів у їх виробників. Якщо пацієнт страждає на клаустрофобію, то може застосовуватися легка седація або візуалізація за допомогою сканерів з відкритим контуром. Однак більшість таких апаратів дозволяють отримувати знімки більш низької якості. У рідкісних випадках відзначаються алергічні реакції на введення контрастної речовини для МРТ.
особливі міркування
Деяким пацієнтам (в критичному стані і тим, яким недавно був проведений тромболізис) застосування МРТ не цілком підходить, так як під час проведення дослідження немає можливості оцінки їх клінічного стану. Якщо МРТ все ж вкрай необхідна, то її проводять з мінімальним необхідним для встановлення діагнозу набором послідовностей, наприклад Т1, Т2, ДВІ або ПВІ і МР-ангіографія. У багатьох клініках розроблені спеціальні протоколи по ОІІ, спрямовані на мінімізацію тривалості обстеження. Пацієнтів, яким планується проведення МРТ, слід оцінювати на предмет наявності протипоказань, таких як клаустрофобія, металеві імплантати, водії ритму і МР-несумісні штучні серцеві клапани.
Resoundant оголошує про партнерство з United Imaging
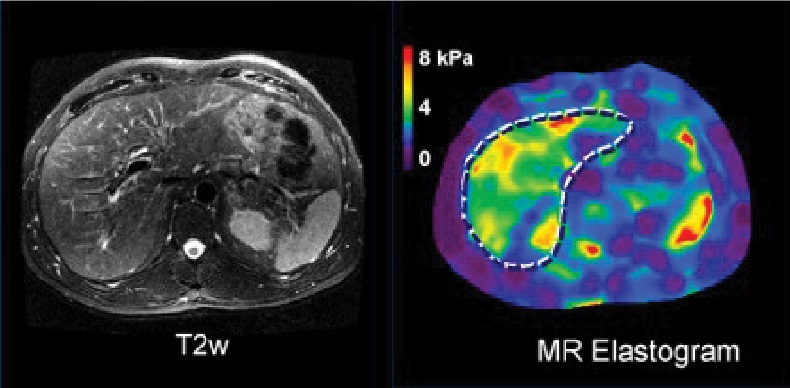
30 листопада 2020 р. – компанія Resoundant Inc. оголосила, що уклала стратегічне партнерство з United Imaging Healthcare, щоб розпочати пропонувати вдосконалену магнітно-резонансну еластографію (MRE) на провідних системах МРТ United Imaging.
Місія United Imaging охоплює відданість останнім інноваціям та забезпечення їхньої доступності у всьому світі. Унікальна модель компанії “все в” має найвищі пріоритетні програми, необхідні для задоволення щоденних робочих процесів. Включення MRE як основного продукту буде прикладом цього стандарту, оскільки він став важливим клінічним інструментом для неінвазивної оцінки фіброзу печінки у всьому світі.
“Ми раді співпраці з United Imaging, щоб забезпечити MRE на їхніх передових рішеннях з МР”, – сказала Кеті Андерсон, JD , головний операційний директор Resoundant. “Це партнерство сприятиме нашій всеохоплюючій місії: кардинально просунути допомогу пацієнтам шляхом дослідження, розробки та розповсюдження високоефективних програм МР-еластографії”.
Віддзеркалюючи відданість проривним технологіям, дві компанії також домовились працювати над впровадженням наступного покоління MR Elastography, що називається 3D-MRE , як стандартний продукт для систем 1,5 і 3,0 Т.
“Якщо ми розглянемо прийняття MRE до цього часу, багато країн Азіатсько-Тихоокеанського регіону зробили величезну роботу, забезпечивши доступ до MRE”, – сказав Майкл Калуткевич , віце-президент з питань глобальної політики та комунікацій Resoundant. “Наше партнерство з United Imaging забезпечить ще більшій кількості пацієнтів доступ до прогресивного МРТ”.
Наразі дві компанії перебувають на завершальній стадії випробувань та впровадження з метою постачання в 2021 році.
Про візуалізацію MR за хронічної хвороби печінки
Кількісні технології візуалізації пропонують потужні можливості для вирішення глобальної проблеми хронічного захворювання печінки. Для багатьох пацієнтів МРВ може служити надійною, менш дорогою та безпечною альтернативою біопсії для діагностики та стадії фіброзу печінки.
Технічні переваги MRE для оцінки фіброзу та PDFF для оцінки жиру в печінці були добре підтверджені в десятках досліджень проти парних біопсій, з високим ступенем згоди між читачами та повторюваності. Обидва біомаркери також стандартизовані на різних платформах постачальників та потужності поля та використовують однакові кількісні обмеження незалежно від основної етіології (вірусний гепатит, жирова хвороба печінки тощо), що робить їх ідеальними для клінічних досліджень. Ні на одне, ні на інше суттєво не впливають загальні супутні захворювання, які можуть спричинити невдачу в додаткових методах на основі УЗД, таких як ожиріння.
Про MRE
Еластографія МР була винайдена в клініці Мейо. Він широко доступний для клініцистів у понад 1600 місцях по всьому світу і є єдиною технологією МРТ, яка була затверджена для постановки на фіброз печінки. Клініцисти та пацієнти можуть знайти місцезнаходження США на MRE: підключитися . Роль MRE все більше визнається в мультидисциплінарних клінічних рекомендаціях щодо рутинної оцінки фіброзу печінки, особливо у підозрі на випадки неалкогольної жирової хвороби печінки (NAFLD) та неалкогольного стеатогепатиту (NASH). Американський коледж радіології видав Критерії відповідності, які визначають MRE як найбільш точний та застосовний неінвазивний іспит на фіброз печінки. MRE відшкодовується за кодом CPT категорії I (76391) і покривається численними державними та приватними планами страхування.
КТ в оцінки дінаміки перебігу COVID-19: терапія з використанням цитокінової сорбції і селективної плазмофільтрації
В конце 2019 года в Китае произошла вспышка новой коронавирусной инфекции с эпицентром в городе Ухань, провинция Хубэй. Международный комитет по таксономии вирусов дал официальное название возбудителю инфекции SARS-CoV-2, а Всемирная организация здравоохранения присвоила официальное название заболеванию, вызванной новым коронавирусом, –COVID-19 («Coronavirus disease 2019»).
По тяжести течения отмечаются различные формы этого заболевания от бессимптомных до тяжелых, которые могут приводить к летальному исходу. Согласно одной из теорий, тяжелые формы течения COVID-19 могут быть связаны с чрезмерной реакцией иммунной си-стемы организма, называемой «цитокиновым штормом». Когда вирус SARS-CoV-2 попадает в легкие, он привлекает иммунные клетки в зону повреждения, что приводит к локализованному воспалению. В некоторых случаях происходит неконтролируемая чрезмерная вы-работка цитокинов, которые активируют большое количество иммунных клеток, происходит гипервоспаление. Такая дисрегуляция иммунного ответа приводит к повышенной проница-емости капилляров, дыхательной недостаточности в результате прогрессирующего повреждения легких, острому респираторному дистресссиндрому и полиорганной недостаточности [3]. Лабораторными признаками «цитокинового шторма» являются тромбоцитопения и лейкопения, а также повышение следующих показателей: ферритина, С-реактивного белка (СРБ), триглицеридов, лактатдегидрогеназы, АЛТ, АСТ, билирубина, фибриногена, D-димера, интерлейкина 6 (IL-6) [3, 4]. В настоящее время всем пациентам стяжелой формой COVID-19 рекомендуется проводить лабораторный скрининг уровней медиаторов гипервоспаления.
Существуют различные способы коррекции «цитокинового шторма». Терапевтические варианты включают использование стероидов, внутривенного иммуноглобулина, селективную блокаду цитокинов и ингибирование янускиназ [5]. Так, результаты многоцентрового исследования продемонстрировали эффективность препарата тоцилизумаб (блокатор рецептора IL-6) у больных COVID-19 [8]. Особый интерес представляют методы механического очищения крови от медиаторов воспаления такие, как цитокиновая сорбция и селективная плазмофильтрация.
Для определения эффективности различных методов лечения, оценки динамики состояния больного методом выбора может стать компьютерная томография (КТ), которая позволяет объективно характеризовать повреждение легочной ткани.
Клиническое наблюдение
Приводим клинический случай пациента В., 59 лет, который поступил в COVID центр на базе Национального медицинского исследовательского центра кардиологии (НМИЦ кардиологии) 02.05.2020 г. с жалобами на повышение температуры тела до 38,7ᵒС, сухой кашель, слабостьи потерю обоняния. Больным себя считает с 29.04.2020 г., когда впервые отметил усебя повышение температуры тела до 37,2ᵒС. Втот же день пациент был осмотрен врачом, амбулаторно начата терапия Амоксиклавом, произведен забор назофарингеального мазка для ПЦР на SARS-CoV-2. В связи с ухудшением самочувствия больного, нарастанием лихорадки до 38ᵒС02.05.2020 г. больному амбулаторно была выполнена КТ органов грудной клетки, по результатам которой выявлены признаки двусторонней полисегментарной вирусной пневмонии с вовлечением до 10% легочной паренхимы (КТ-1). Больной был госпитализирован в НМИЦ кардиологии с предварительным клиническим диагнозом: «Внебольничная двусторонняя пневмония. Подозрение на коронавирусную инфекцию».
Из анамнеза стало известно, что сопутствующих хронических заболеваний у больного не было. Объективный статус при поступлении: состояние средней степени тяжести; кожные покровы чистые, обычной окраски; ЧСС = 81 в минуту; ЧДД = 20 в минуту; АД = 122/72; SpO2 = 96% на атмосферном воздухе; температура тела 38,1ᵒС. По результатам лабораторных исследований отмечалось выраженное увеличение уровня СРБ= 193,1 мг/л.
Согласно действовавшим рекомендациям была инициирована терапия: Гидроксихлорохин 400 мг/сутки, Азитромицин 500 мг/сутки, продолжен прием Амоксиклава 2 г/сутки. Для профилактики тромбо эмболических осложнений был назначен Эноксапарин Натрия 40 мг.
Кроме того, была назначена Джакави 5 мг 2 раза в сутки per os для предотвращения «цитокинового шторма». Однако, в связи с развитием побочных эффектов в виде головокружения, тошноты и мучительного кашля с рвотой, было принято решение об отмене Джакави и применении препарата Эфлейры 120 мг подкожно.
Несмотря на проводимое лечение в после-дующие дни состояние больного стало ухудшаться: стойко сохранялась и нарастала лихорадка (до 39,3ᵒС), появилась дыхательная недостаточность ввидетахипноэдо30 в минуту, показатели сатурации крови снижались: SpO2 = 89% на атмосферном воздухе; 93% на фоне инсуффляции увлажненного кислорода через носовые канюли 5 л/мин. В анализах крови отмечалось увеличение уровня СРБ = 224 мг/л и IL-6 = 449 пг/мл.
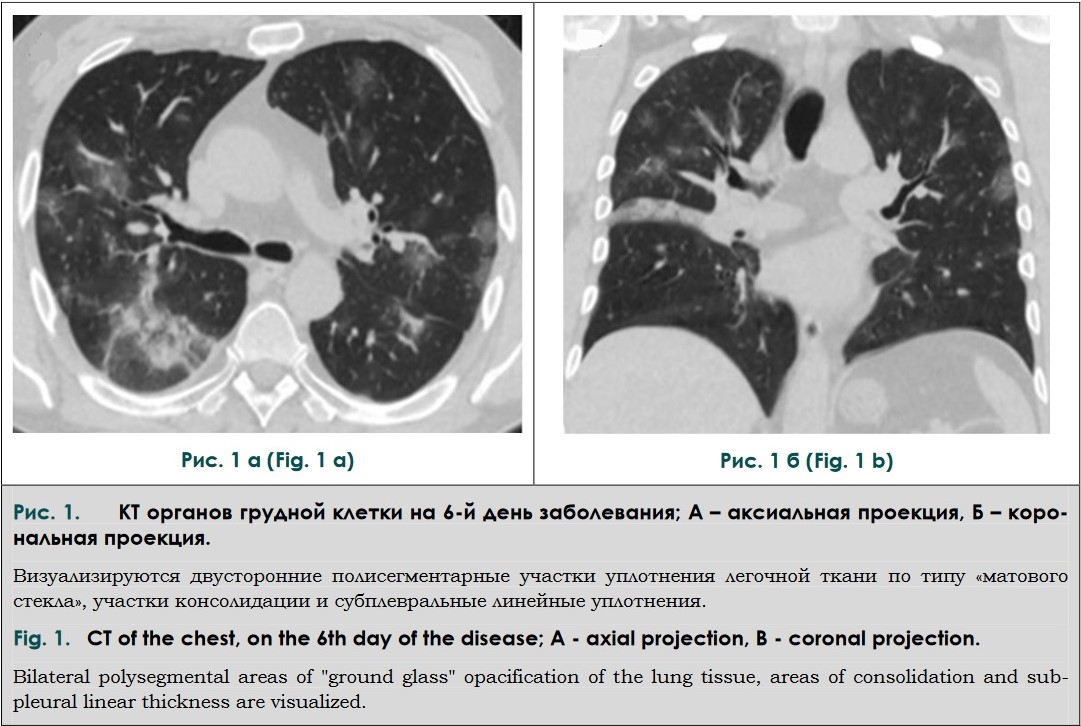
На третий день госпитализации была про-ведена КТ органов грудной клетки (от 04.05.2020 г.), по результатам которой отмечалась отрицательная динамика (рис. 1). Были выявлены множественные двусторонние полисегментарные участки уплотнения легочной ткани по типу «матового стекла», расположенные преимущественно субплеврально и перибронхиально, небольшие участки консолидации легочной ткани и субплевральные линейные уплотнения. Поражение легочной ткани составляло около 40% и соответствовало средней степени тяжести КТ-2.
05.05.2020 г. пациенту был введен ингибитор интерлейкина Сарилумаб 200 мг в качестве иммуносупрессора. Однако продолжала нарастать дыхательная недостаточность (ЧДД = 40 в минуту) с десатурацией крови (SpO2 = 84%), в связи с чем, 07.05.2020 г. больной был переведен в ПРИТ.
07.05.2020 г. и 08.05.2020 г. в условиях ПРИТ больному было проведено 2 сеанса цитокиновой сорбции и селективной плазмофильтрации с использованием аппарата «Гемма», сорбционной колонки HA330 (Jafron) и плазменного фильтра Evaclio 2C (скорость перфузии 115 мл/мин, объем эффлюента 23% от общего объема перфузированной крови). Кроме того, в течение трех дней проводилась СРАР-терапия, которая заключается в обеспечении постоянно-го положительного давления в дыхательных путях при помощи специальных компрессоров. На этом фоне была отмечалась положительная д-намика лабораторных показателей в виде снижения уровней СРБ = 84 мг/л, IL-6 = 258 пг/мл, нормализовалась температура тела до 36,3ᵒС, однако, сохранялась гипоксемия (SpO2 = 87% на атмосферном воздухе, 97% на фоне инсуффляции увлажненного кислорода через носовые канюли 10 л/мин).
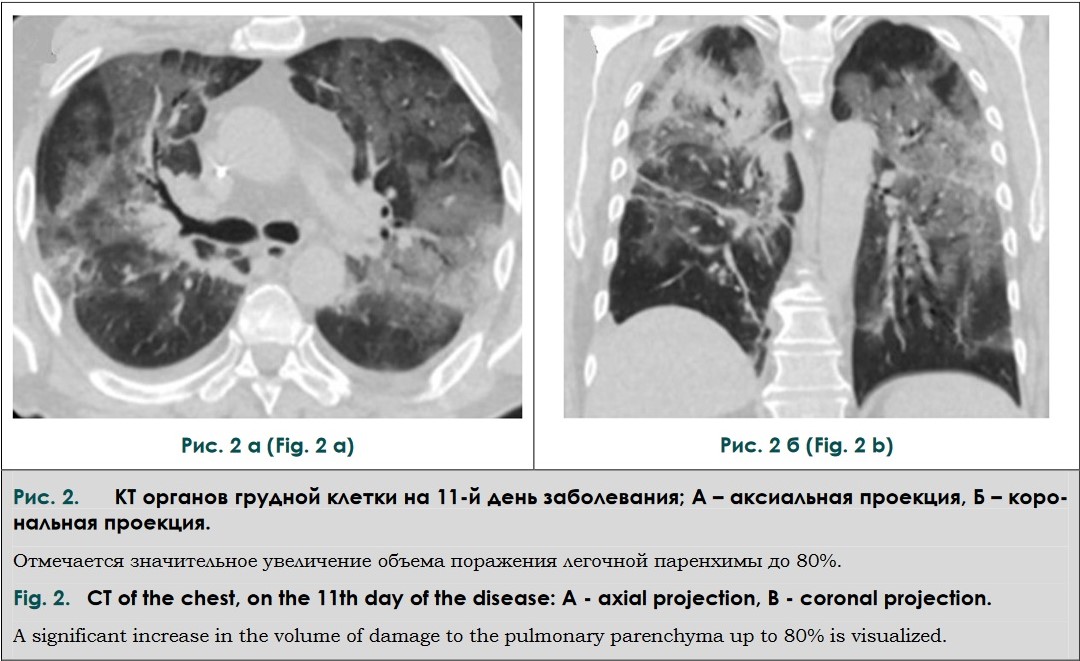
09.05.2020 г. была выполнена КТ органов грудной клетки, по результатам которой отмечалась отрицательная динамика в виде значительного увеличения объема поражения легочной паренхимы до 80% от объема легких, что соответствует критической степени тяжести КТ-4. Инфильтративные изменения приобрели диффузный характер и сочетались с ретикулярными изменениями. Кроме того, отмечалось появление умеренного количества жидкости в плевральных полостях (рис. 2).
В связи с ухудшением состояния больного по данным КТ была начата терапия Дексаметазоном 16 мг в сутки в течение 3-х дней с после-дующей постепенной отменой. На этом фоне была отмечена положительная динамика клинико-лабораторных показателей: СРБ = 1 мг/л, IL-6 = 2,4 пг/мл, температура тела 36,5ᵒС, SpO2 = 93% на атмосферном воздухе.
По результатам КТ органов грудной клетки от 15.05.2020 г. также была зафиксирована положительная динамика. Определяемые ранее зоны инфильтрации легочной ткани уменьшились в размерах, стали менее плотными, с трансформацией в сетчатые ретикулярные уплотнения и участки консолидации. Объем поражения легочной ткани уменьшился до 45%, что соответствует средней степени тяжести КТ-2 (рис. 3).

С учетом улучшения клинического состояния, нормализации уровня воспалительных маркеров, сохраняющейся нормальной температуры тела, положительной динамикой по данным КТ органов грудной клетки больной был выписан из стационара27.05.2020 г. (26-й день заболевания) для дальнейшего наблюдения и лечения в амбулаторных условиях.
Обсуждение
Новая коронавирусная инфекция SARS-CoV-2 за короткие сроки получила широкое распространение и стала причиной масштабной пандемии заболевания COVID-19. Болезнь часто сопровождается развитием вирусной пневмонии и ее тяжесть напрямую зависит от степени поражения легочной ткани. КТ играет важную вспомогательную роль в первичной диагностике COVID-19, обладая более высокой чувствительностью в сравнении с ПЦР к SARS-CoV-2 (98% против 71%) и дополняя данный метод тестирования [10]. Кроме того, КТ может служить надежным методом мониторинга развития заболевания и оценки эффективности терапии.
Несмотря на то, что группу риска тяжелого течения COVID-19 составляют в основном пациенты старшего возраста и люди, имеющие сопутствующие хронические заболевания, из-вестны случаи быстрого прогрессирования заболевания с развитием острого респираторного дистресс-синдрома вплоть до летального исхода у лиц молодого и среднего возраста. По некоторым данным, это может быть связано с «цитокиновым штормом». В настоящее время изучаются различные способы коррекции этого состояния у больных COVID-19, включая медикаментозную терапию и методы механиче-ского очищения крови от маркеров воспаления. При этом для мониторинга состояния больного и эффективности проводимой терапии могут применяться результаты КТ.
В данном клиническом примере представлен случай тяжелого течения COVID-19 у пациента 59 лет без сопутствующих хронических заболеваний, у которого отмечалась прогрессирующая двусторонняя пневмония. В ходе лечения были использованы различные терапевтические варианты ликвидации «цитокинового шторма», а также методы цитокиновой сорбции и селективной плазмофильтрации. Оценка эффективности терапии и мониторинг состояния больного проводились на основании данных клинико-лабораторных исследований и КТ органов грудной клетки. На определенном этапе лечения было отмечено несоответствие клинико-лабораторных показателей и результатов лучевого исследования: нормализации температуры тела, снижения уровней СРБ и IL-6 сопровождались отрицательной динамикой КТ-картины органов грудной клетки в виде значительного увеличения объема поражения легочной паренхимы до 80% от объема легких, что соответствовало критической степени тяжести КТ-4. Благодаря своевременному выявлению ухудшения состояния больного и коррекции терапии удалось достичь регресса клинических проявлений заболевания. Таким образом, КТ может служить методом выбора для оценки эффективности лечения при COVID-19, помогая оперативно и объективно оценить степень тяжести заболевания.
Заключение
Представленный клинический случай демонстрирует важную роль КТ органов грудной клетки как в первичной диагностике COVID-19, так и для последующего динамического мониторинга состояния больного и оценки эффективности лечения.




