Вступ
Загальні дані
Магнітно-резонансну томографію (МРТ) все частіше застосовують в діагностиці гострого ішемічного інсульту (ОІІ). Мета цієї статті – простим і доступним чином викласти сучасні дані про застосування МРТ в діагностиці ОІІ. МРТ – метод візуалізації, який швидко розвивається і дозволяє з досить високою специфічністю виявляти зміни, пов’язані з інсультом. Звичайно, він має і недоліки, такі як висока вартість, тривалість проведення дослідження і більш низька чутливість до субарахноїдальним крововиливом. Недавні досягнення, такі як підвищена потужність магнітного поля (1,5-3 Т), нові послідовності візуалізації і апарати з відкритим контуром для пацієнтів з клаустрофобію і ожирінням сприяють ще більшому поширенню методики в діагностиці ОІІ.
Патологічна фізіологія
При попаданні в сильне магнітне поле деякі ядра атомів тіла людини переходять в збуджений стан; вони адсорбують радіочастотну енергію магнітного поля і потім віддають її при повній релаксації. Енергія вивільняється з збудженої тканини протягом короткого періоду часу відповідно до однієї з двох констант релаксації – Т1 і Т2 послідовностей, а яку випромінює енергія конвертується в зображення. Контрастність останніх обумовлена різною інтенсивністю випромінюваних сигналів, яка в свою чергу пов’язана з різною концентрацією ядер в тканинах організму.Водень (протони) – один з найбільш поширених атомів в тканинах людського організму. Застосовувалися й інші органічні субстанції, але вони дозволяють отримати меншу просторову роздільну здатність. Вивчаються біохімічні склади, такі як лактат і N-ацетил аспартат, з тим, щоб зрозуміти значущість різних концентрацій цих компонентів при різних патологічних станах (магнітно-резонансна спектроскопія (МРС)).Найбільш часто вживані види МР-візуалізації такі:
- Т1-зважені зображення (Т1ВІ), на яких ліквор (цереброспінальної рідина) має низьку інтенсивність сигналу в порівнянні з мозковою тканиною;
- Т2-зважені зображення (Т2ВІ), на яких ліквор має більш інтенсивний сигнал в порівнянні з мозковою тканиною;
- зображення, зважені по спінової щільності, при яких ліквор має однакову щільність з мозком;
- послідовності градієнтного відлуння, які дозволяють з високою чутливістю виявляти ранні геморагічні зміни;
- дифузно-зважена візуалізація (ДВВ), при якій на зображеннях видно випадкові мікроскопічні руху молекул води;
- перфузійному-зважені зображення (ПВІ), на яких гемодинамически зважені МР-послідовності грунтуються на проходженні контрасту через мозкову тканину.
Патогенез формування знахідок, виявлених при візуалізації
Незалежно від причини ішемія нейронів призводить до виснаження внутрішньоклітинних запасів аденозинтрифосфорної кислоти (АТФ), в результаті чого порушується робота пов’язаних з мембраною АТФ-залежних іонних каналів, які відповідальні як за підтримку мембранних потенціалів спокою, так і за генерацію потенціалів дії. Ці мембранні аберації призводять до накопичення іонів всередині клітини (включаючи кальцій), і таким чином створюється градієнт, що обумовлює накопичення води і розвиток цитотоксического набряку клітини.Мозкові ендотеліальні клітини мають більш високу резистентність до ішемії, ніж нейрони і глия. Приблизно через 3-4 годин після розвитку ішемії цілісність гематоенцефалічного бар’єру порушується і протеїни плазми крові починають потрапляти в позаклітинний простір. Потім, після реперфузії, за ними слід вода, що призводить до розвитку вазогенного набряку; цей процес починається через 6 годин після інсульту і досягає максимуму на 2-4-й день. Реперфузія також може супроводжуватися геморагічної трансформацією вогнища інфарцірованія, що найчастіше буває при великих кортикальних інфарктах.Зміни на МР-зображеннях, пов’язані з ОІІ, розташовуються в зоні кровопостачання закупорити судини, що в цілому типово для цереброваскулярної патології і корисно при диференціальної діагностики.
Летальність і інвалідизація
Застосування клінічних даних та даних МРТ для прогнозування результатів ОІІ
ДВІ дозволяє оцінити ядро інфаркту, а ПВІ – ішемічну півтінь ( «пенумбра»). Невідповідності цих зображень і є та тканину, яка потенційно залишиться живий після реперфузії. Але, незважаючи на дані на користь «гіпотези невідповідності», немає переконливих даних про те, що лише тільки наявність такої невідповідності дозволяє виявити пацієнтів, які дадуть відповідь на терапію. Недостатня стандартизація може бути однією з проблем.RRE-90 – проста прогностична шкала, в якій враховуються клінічні і візуалізаційні дані, що дозволяють оцінити ранній ризик розвитку повторного інсульту в гострий період ОІІ (табл. 1). Було показано, що RRE-90 має гарну предиктивної силою, і якщо зовнішні дослідження верифікують ці дані, то її можна буде застосовувати для створення індивідуалізованих алгоритмів лікування пацієнтів (табл. 2).

рентгенографія
З метою виявлення металевих імплантатів і чужорідних тіл (водії ритму, судинні кліпси, штучні серцеві клапани і ін.) Іноді проводять звичайну рентгенографію.
методики МРТ
Дифузно-зважена візуалізація
ДВВ чутлива до мікроскопічних випадковим рухам протонів води – коефіцієнт дифузії (ADC, від англ. Apparent diffusion coefficient), який як раз і визначається за допомогою цього методу візуалізації. Молекули води рухаються у напрямку градієнта магнітного поля; вони накопичують фазовий зсув, який має пряме відношення до ослаблення зображення.У численних дослідженнях було показано, що ADC ішемічних зон на 50% і більше менше, ніж аналогічні показники нормальних зон мозку. На дифузно-зважених зображеннях (ДВІ) вони виглядають як яскраві (гіперінтенсивні) ділянки (рис. 1). Показано, що зміни ADC відбуваються вже через 10 хв після розвитку ішемії.
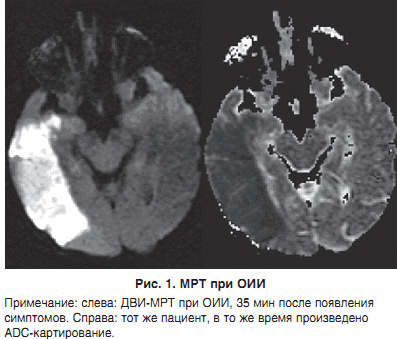
Цитотоксичний набряк розвивається внаслідок порушення функції калій-натрієвих насосів, яке в свою чергу є наслідком метаболічних порушень, пов’язаних з ОІІ; це відбувається протягом декількох хвилин після розвитку ішемії і призводить до підвищення обсягу води в церебральної тканини на 3-5%. Передбачається, що зниження інтенсивності руху молекул води між поза- і внутрішньоклітинним простором є причиною зниження показника ADC.Дифузія молекул води регулюється біологічними бар’єрами (наприклад клітинними мембранами і органеллами). Поведінка молекул води несиметрично і при вимірюванні ADC в одному напрямку розподіл може бути нерівним; це може створювати неправильне уявлення про патологічному вогнищі. Показник ADC вимірюють в кількох напрямках (3, 6 або більше), а картування його виробляють з тим, щоб отримати незалежні від напрямку дані про дифузії. При вимірі ADC в 6 або більше напрямках можна розрахувати рух всіх молекул води ( «тензорна матриця») – повне дифузне тензорне картування, яке можна застосовувати для візуалізації шляхів білої речовини.Зниження ADC може відзначатися при інших станах, таких як глобальна ішемія, гіпоглікемія і епілептичний статус; тому слід брати до уваги клінічний стан пацієнта.У дослідженнях, проведеному у людей, було показано, що пошкодження в зонах зі зниженим ADC дуже рідко оборотні, хоча в декількох дослідженнях повідомлялося, що інтраартеріальний тромболізис іноді призводить до регресу дифузійних дефектів. Методикою, яку найчастіше застосовують для отримання ДВІ, є ультрашвидкий ехопланарная візуалізація (ЕПШ); вона дозволяє значно зменшити тривалість сканування і нівелює рухові артефакти.Різке зниження показника ADC поступово приходить в норму на 5-10-й день після розвитку ішемії (псевдонормалізація); згодом він навіть перевищує нормальні значення, що іноді дозволяє відрізняти гострі, підгострі і хронічні вогнища.ДВІ має дуже високу чутливість і відносної специфічністю у виявленні ОІІ; проте в недавніх дослідженнях було показано, що дрібні лакунарні інфаркти можуть бути втрачені. Нормальні результати ДВ-МРТ у пацієнта З ІНСУЛЬТОПОДІБНИМ симптомами повинні направляти лікаря на пошук інших неішемічної причин симптомів. Аномалії дифузії відзначаються практично у 50% пацієнтів, які перенесли ТІА.На підставі клінічного досвіду співробітників інсультного центру Chapel Hill Університету Північної Кароліни, диференціація гіперінтенсивного зон при ДВІ виглядає наступним чином:
- підгострий ішемічний інсульт – гіперінтенсивного регресує через 7-14 днів;
- геморагічний інсульт – зазвичай світлий на Т1ВІ;
- бляшки при розсіяному склерозі – також світлі на FLAIR-зображеннях і Т2ВІ;
- травма голови – травма в анамнезі;
- абсцес головного мозку – посилення вогнища у вигляді кільця при візуалізації з контрастом;
- судинні сплетення – зазвичай розташовуються всередині шлуночків, можуть бути двосторонніми;
- епідермоід – зазвичай локалізується екстрааксіально;
- повітря в кістки – зазвичай з двох сторін, в скроневої кістки.
Перфузійному-зважена візуалізація
Ця методика дозволяє отримати дані про перфузії головного мозку. Найбільш часто вживаним методом є болюс-контрастний трекінг, при якому візуалізація ґрунтується на моніторингу недіффундірующего контрастної речовини (гадоліній), що проходить через мозкову тканину.У міру проходження контрасту через зону інфарцірованія інтенсивність сигналу знижується і потім стає нормальною в міру переходу до здорової тканини. Крива, отримана на підставі цих даних ( «крива розмитості сигналу» від англ. Signal washout curve), відображає і дозволяє оцінити обсяг крові в мозку (ОКМ, син. «Церебральний об’єм крові»).Функцію артеріального припливу можна виміряти на нижніх зрізах або за допомогою вимірювання концентрації гадолінію, яка пропорційна змінам на Т2ВІ при введенні контрасту в низьких дозах (<3 мг / кг). На підставі цих даних можна отримати кількісні карти мозкового кровотоку (МК), ОКМ, середнього часу транзиту (СВТ) і часу до пікових показників (ВДП), а також багато інших гемодинамічні параметри. Ведуться дискусії про те, які параметри ПВІ необхідно використовувати. У більшості центрів США застосовують такі показники, як СВТ і ВДП.Було показано, що ДВІ і ПВІ – більш ефективні методи діагностики ОІІ, ніж рутинна МРТ, як в гострій фазі захворювання, так і протягом 48 годин після події. Дуже важливо застосовувати обидві ці техніки, так як разом вони дозволяють отримати інформацію про локалізацію і поширеність зони інфарцірованія вже в перші хвилини після розвитку інсульту; при повторному проведенні методики дозволяють відслідковувати розвиток ішемічного вогнища. Ці дані можуть мати велике значення при виборі методу лікування, а також в прогнозуванні результатів захворювання.Протягом декількох днів на повторних ДВІ вогнище зазвичай збільшується. Передбачалося, що цей процес можна зупинити, якщо рано провести реперфузію. Невеликі осередки на ПВІ зазвичай не збільшуються.Дифузійно-перфузионное невідповідність зазвичай являє собою ішемічну півтінь – зону неповної ішемії, яка лежить безпосередньо біля ядра зони інфарцірованія. Пенумбра розглядають як життєздатну область, яка, однак, знаходиться під загрозою ішемії; її можна врятувати, якщо швидко провести необхідні втручання. Життєздатність цієї зони зберігається до 48 год після розвитку ОІІ. Визначення обсягу ішемічної півтіні може бути корисним при відборі пацієнтів для проведення тромболітичної терапії і можливо навіть для таких рутинних методів, як каротидної ендартеректомія та підвищення артеріального тиску. Це також може бути корисно в визначенні співвідношення ризик / користь від застосування цих методів лікування (рис. 2).
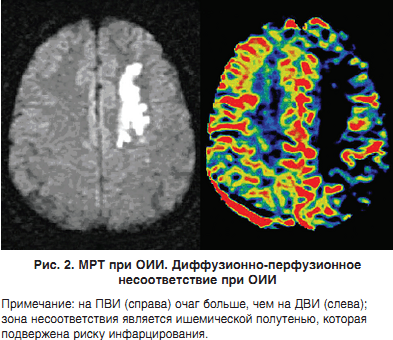
Недоліки показника диффузионно-перфузійного невідповідності в основному методологічні та включають: (1) недостатнє анатомічне відповідність ПВІ і ДВІ; (2) різну чутливість ПВІ в залежності від затримки Тmax; (3) візуальну оцінку невідповідності.МРТ досі має деякі обмеження до застосування, зокрема у пацієнтів з металевими імплантатами та у пацієнтів в критичному стані, яким необхідний постійний моніторинг.Ці нові методи – ДВІ і ПВІ – є найбільш перспективними галузями застосування МРТ щодо їх можливостей виявляти ранні зміни (перші хвилини після інсульту). В даний час їх застосовують в клінічних дослідженнях для оцінки ефективності тромболітичної і нейропротектівний терапії у пацієнтів з ОІІ.
МРТ, залежне від концентрації кисню крові (BOLD – blood oxygen level-dependent)
Фракція екстракції кисню (ФЕК), яку визначають за допомогою позитронно-емісійної томографії, вважається стандартом візуалізації ішемічної півтіні при ОІІ. До сих пір МР-ДВ / ПВ-візуалізація є єдиною МР-методикою, яка дозволяє оцінити зону оборотного пошкодження мозку.BOLD є новим методом, який дозволяє визначати деоксігемоглобін в церебральних капілярах і венах як МР-індикатор церебральної ФЕК. За даними недавніх досліджень, BOLD-МРТ дозволяє більш ефективно оцінити ішемічну півтінь при ОІІ, ніж показник МР-ПВ / ДВ-невідповідності. Для розуміння клінічного значення цього методу візуалізації потрібні подальші дослідження.
Ехопланарная візуалізація
ЕПШ є новим методом, який можна застосовувати для візуалізації фізіологічних процесів і оцінки коефіцієнтів дифузії ишемизированного мозку. Зміни церебральної оксигенації можна проводити моніторинг за допомогою послідовностей градиентного луни і ЕПШ, на яких деоксігенірованная кров поводиться як контрастну речовину.ЕПШ можна застосовувати в поєднанні з введенням контрастної речовини з метою оцінки церебральної перфузії і функціональних змін ОКМ.При використанні цього варіанту візуалізації зони гіпоперфузії після ін’єкції контрастної речовини виглядають гіперінтенсивного. Ця методика менш витратна за часом.
Магнітно-резонансна спектроскопія
МРС є одним з недавніх технологічних досягнень в області МР-технологій; метод дозволяє оцінити метаболічну активність і концентрації деяких метаболітів в специфічних областях мозку. Проводилися спектроскопічні дослідження із застосуванням протонів і фосфору.МРС дозволяє виявити зниження вмісту N-ацетил аспартату, який вважається маркером нейронів і є найбільш частим ознакою при гострому інсульті. Цей стан може розвинутися протягом декількох годин після розвитку інсульту і потім продовжуватися в підгострій і хронічній фазах інсульту, ймовірно, через втрату нейронів. Підвищення вмісту лактату – ще одна важлива ознака, який пояснюють анаеробним метаболізмом ішемізованої тканини. Дослідження інших метаболітів, таких як холін і креатин, показали зниження їх рівня при ОІІ.Фосфорна спектроскопія дозволяє отримати інформацію про енергетичну метаболізмі і pH, виснаженні запасів АТФ, зниженні тканинного pH і підвищенні співвідношення неорганічних фосфатів та фосфокреатину; це було показано як в клінічних, так і в експериментальних дослідженнях.Велика тривалість дослідження, слабкість сигналу і низьке просторову роздільну здатність є основними обмеженнями застосування МРС в клінічній практиці для оцінки церебральної ішемії; проте в ряді публікацій повідомляється, що результати МРС можуть мати при ОІІ прогностичне значення.
Магнітно-резонансна ангіографія
Магнітно-резонансна ангіографія (МРА) дуже чутлива до потоку і грунтується на відмінностях сигналу між рухомою кров’ю і нерухомою тканиною мозку; в результаті можна отримати ангіограммоподобние зображення судин шиї та голови.Метод МРА важливий в діагностиці розшарувань, причому на зображенні можна побачити як помилковий, так і справжній просвіт ураженої судини. Далі буде наведено короткий опис двох основних методик.Тривимірна часопролітної методика (від англ. 3D time-of-flight, 3D-TOF) ґрунтується на посиленні, пов’язаному з потоком; це кращий метод. Тим не менш, він має деякі недоліки, одним з яких є втрата сигналу від турбулентного потоку крові в звивистих і стенотично сегментах судин, що ускладнює оцінку стенозу в цих областях. Останні є найбільш частими вогнищами локалізації атеросклеротичних уражень. Крім того, в зонах з повільним кровотоком спінова насиченість сканів призводить до переоцінки стенозу. При проведенні дослідження з контрастуванням можна отримати більше інформації, ніж при стандартній ангіографії, особливо у виявленні критичних стенозів позачерепних судин, але метод менш надійний в діагностиці інтракраніальних критичних стенозів. Завжди треба пам’ятати про те,Двомірна TOF-МРА (2D-TOF) також грунтується на відносній контрастності між поточною кров’ю і нерухомою тканиною. Метод дозволяє отримати більш якісні зображення, ніж 3D-TOF МРА, в зонах з низькою швидкістю кровотоку. 2D-TOF-зображення при візуалізації патологічних змін зони біфуркації сонних артерій добре корелюють з даними каротидної ангіографії. Однак недоліками методики є часто відзначаються значні артефакти, які ускладнюють оцінку деталей, і тривалий час сканування.Модифікована TOF-МРА-методика, в якій застосовують множинне накладення тонких зрізів (multiple overlapping thin slab acquisitions – MOTSA), поєднує в собі переваги 2D і 3D TOF МРА. Метод виключно інформативний при візуалізації важкого стенозу, однак ступінь стенозу може кілька переоцениваться.Двомірна фазово-контрастна МРА є методикою, яка корисна при специфічної диференціації повільного кровотоку і його відсутності і нормального струму крові; вона захоплює лише тільки дійсно діючі судини. Для того, щоб не упустити деякі патологічні зміни, наприклад паравазального гематоми (які невізуалізіруются цим методом), поряд з фазово-контрастної МРА слід застосовувати інші послідовності візуалізації, такі як спіновий або градиентное відлуння. Ще одним недоліком фазово-контрастної МРА є втрата сигналу при турбулентному потоці в звивистих судинах.
типи інфарктів
тромбоемболічний інфаркт
Є найбільш частим варіантом. Зазвичай на МРТ вогнище виглядає клинообразно, розташовуючись в зоні кровопостачання будь-якої артерії. Недавні дані підтримують гіпотезу про те, що одиничний інфаркт в будь-якій зоні кровопостачання швидше тромботический, а множинні – скоріш за емболіческіе.
Інфаркти в «вододільних» зонах (в суміжних зонах кровопостачання)
Цей варіант розвивається в дистальних відділах зон кровопостачання окремих артерій. Він може розташовуватися як поверхнево, так і глибоко в мозковій паренхімі. Типові причини такого варіанту інсульту включають гіпотензію, зупинку серцевої діяльності і дихання, проксимальний стеноз артерії або її оклюзію. На МРТ при цьому відзначається неповний тромбоемболічний ішемічний інфаркт і раннє посилення паренхіми, що говорить про розвиток ранньої реперфузії. Відповідно до нових даних, цей тип інфаркту більш ефективно можна візуалізувати за допомогою ДВІ.
лакунарний інфаркт
Вважають, що ці маленькі глибокі церебральні інфаркти виникають через ураження дрібних судин, обумовленого ліпогіалінозом і фібриноїдним некрозом; їх найчастіше відзначають в осіб з гіпертензією або на цукровий діабет. Вогнища зазвичай локалізуються в базальних ядрах, внутрішньої капсулі, таламусі, стовбурі мозку і мозочку. Патерн візуалізації цих патологічних утворень аналогічний такому при тромбоемболічних інфарктах.
Венозний тромбоз і інфаркт
Оклюзія церебральних вен і венозних синусів зазвичай обумовлена системними станами, такими як вагітність, захворювання сполучної тканини, запальні ураження кишечника і стани, що супроводжуються гіперкоагуляції, але також і місцевими – інфекції, пухлини і травми. Оклюзія венозних структур обумовлює порушення відтоку аж до блокування кровотоку, що в результаті призводить до формування паренхіматозних інфарктів і геморагій. Пацієнтів зазвичай госпіталізують в кінці гострої фази або в підгострій фазі, що ускладнює діагностику, так як встановлення діагнозу в цих випадках залежить від методів візуалізації.Дані МРТ при цих варіантах інсульту включають відсутність сигналу від венозного струму крові, відсутність нормального венозного посилення і виявлення з- або гіперінтенсивного сигналів від венозних структур як в Т1-, так і в Т2ВІ. Ці варіабельні патерни посилення обумовлені різними продуктами крові, які містяться в патологічному вогнищі. Зміни зазвичай двосторонні, вони не відповідають зонам артеріального кровопостачання і часто поєднуються з крововиливами. Тривимірна фазово-контрастна МР-венографія є кращою методикою діагностики і оцінки венозних тромбозів.
Дані МРТ при гострому інсульті
Надгостре період (0-24 год)
МРТ-ДВВ дозволяє виявляти ішемічні зміни через кілька хвилин після їх розвитку. Знижений рух протонів знаходить своє відображення в зниженні показника ADC.На ранніх етапах церебральної ішемії ДВІ із застосуванням контрастування (перший пасаж введеного внутрішньовенно болюсно контрастної речовини) або спінових міток протонів води крові дозволяє виявити зниження мозкового кровотоку і хвилинний об’єм крові (МОК) і підвищення СВТ крові в мозку (рис. 3).
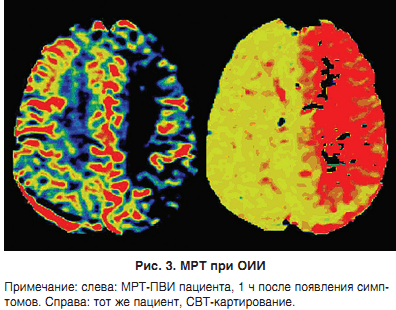
Зона накладення патологічних змін, виявлених при ДВ і ПВ-МРТ, корелює з областю інфарцірованія, в якій сталася необоротна загибель нейронів. Зона невідповідності (зміни в ПВ-режимі більше, ніж в ДВ), як уже говорилося, може бути ішемічної півтіні.Популярним останнім часом підходом є проведення МРТ для виявлення ДВ / ПВ невідповідності з метою відбору кандидатів для проведення лікування поза 3-годинного часового вікна. У двох недавно проведених клінічних дослідженнях ця гіпотеза піддавалася перевірці. У дослідженні DIAS-2 пацієнтам з більш ніж 20% невідповідністю ДВ / ПВ, за даними МРТ, проведеної протягом 3-9 годин після подій, випадковим чином призначали плацебо або десметеплазу. Аналогічним чином було побудовано дослідження EPITHET, але в ньому тимчасове вікно становило 3-6 ч. В обох дослідженнях не вдалося довести, що тромболізис, проведений після 3-годинного терапевтичного вікна, ефективний у пацієнтів з ДВ / ПВ-невідповідністю. У дослідженні ECASS-3 подібний підхід із застосуванням МРТ для відбору пацієнтів не використовувався,EPITHET і DIAS-2 підняли ряд питань технічного властивості, зокрема щодо (1) найбільш адекватного показника співвідношення ДВ / ПВ, (2) адекватного порога ПВ-МРТ, (3) одночасного проведення ДВ- і ПВ-МРТ і (4) автоматичної оцінки невідповідності.Для оцінки зони оборотної ішемії розробляються нові методики МРТ. Одним з таких методів є функціональна BOLD-МРТ.Через кілька годин після розвитку інсульту іноді спостерігається ефект втрати сигналу від судин (30-40% пацієнтів); це найкраще виявляється на T2ВІ.• Через 2-4 ч на Т1ВІ відзначається слабко згладжування борозен внаслідок цитотоксичної набряку.• Через 8 год на Т2ВІ виявляється гіперінтенсівний сигнал як наслідок цитотоксичної і вазогенного набряку.• Через 16-24 год на Т1ВІ відзначається гіпоінтенсівний сигнал внаслідок розвитку як цитотоксического, так і вазогенного набряку.На томограмах з контрастом виявляють артеріальний посилення, за яким слід паренхіматозне. Артеріальний посилення може бути дуже раннім (більш ніж у 50% пацієнтів), і воно обумовлено повільним кровотоком; зазвичай регресує через тиждень.Паренхиматозное посилення відрізняється при повних і неповних інфарктах. При повному інфаркті воно починається на 5-7-й день після інсульту і зберігається протягом декількох місяців. При неповних інфарктах воно може спостерігатися протягом 2-4 ч і зазвичай є більш інтенсивним, ніж при повних інфарктах.Хоча при використанні рутинних МР-послідовностей інсульт в гострій фазі побачити зазвичай не вдається, конвенціональна МРТ дозволяє виявити ознаки внутрішньосудинного тромбозу, такі як відсутність ефекту потоку (ефект «flow void») на Т2ВІ, гіперінтенсівний судинний сигнал в FLAIR-режимі і гіпоінтенсівний судинний сигнал в послідовності градієнтного відлуння (табл. 3).
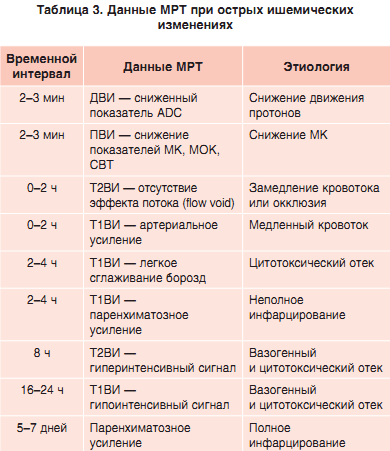
Гостра фаза (1-7 днів)
У цій фазі збільшується набряк, що досягає свого максимального розвитку через 48-72 год, і МР-сигнали стають більш явними і добре відмежовані. Ця ішемічна зона виглядає гіпоінтенсівно на Т1ВІ і гіперінтенсивного на Т2ВІ. У цій фазі можна оцінити мас-ефект.При дослідженні з контрастом артеріальний посилення зазвичай зберігається протягом всієї гострої фази, а паренхіматозне зазвичай оцінюють в кінці цієї фази (при повних інфарктах). При неповних інфарктах паренхіматозне посилення зазвичай відзначається раніше.Під час цього періоду, як правило, розвивається реперфузия і можуть розвиватися петехіальні і більші крововиливи, зазвичай через 24-48 год після розвитку інсульту. Зазвичай петехіальні геморагії є причиною розвитку феномена “затуманення” (fogging phenomenon), що безпосередньо обумовлено продуктами деградації гемоглобіну і маскує інфаркт як на Т1-, так і на Т2ВІ.
Подострая фаза (7-21-й день)
У цій фазі дозволяється набряк і мас-ефект стає менш вираженим; проте інфарцірованного області все ж виглядають гіпоінтенсівно на Т1ВІ і гіперінтенсивного на Т2ВІ. При дослідженні з контрастом артеріальний посилення до цього часу зазвичай регресує, а паренхіматозне ще зберігається протягом всієї фази.
Хронічна фаза (більше 21 дня)
У цій фазі повністю регресує набряк, а інфарцірованного зона все ще виглядає як гіпоінтенсівний вогнище в Т1ВІ і гіперінтенсівний в Т2ВІ. Через загибель тканини в зоні інфаркту відзначається ex vacuo шлуночків, розширення коркових борозен і звивин. На контрастних томограммах паренхіматозне посилення ще зберігається; воно зазвичай проходить через 3-4 міс.
МРТ при ТІА
У 1/3 до половини пацієнтів з ТІА відзначаються патологічні зміни на ДВІ. У багатьох цих випадках відповідні зони на Т2ВІ не виявляються. ПВІ, можливо, є більш чутливим методом, проте він адекватним чином не вивчалось у пацієнтів з ТІА. Характерно, що при виявленні патології на ДВ-МРТ у пацієнтів з ТІА не завжди відзначається инфарцирование на МРТ, проведеної згодом.Хоча ТІА традиційно розглядають як тимчасовий (триває менше 24 годин) неврологічний дефіцит судинного походження, застосування МРТ призвело до переосмислення цього визначення. Чи варто розглядати ДВІ-позитивні випадки ТІА як інсульт, залишається неясним.
МРТ при геморагічному інсульті
Послідовності градієнтного відлуння і ЕПШ дозволяють виявляти клінічно певні мікрокрововиливи, які не видно на рутинних МР і комп’ютерних томограмах. Ці мікрокрововиливи відзначаються у 1 / 5-1 / 4 пацієнтів з ішемічним інсультом і у 5% асимптомних індивідів похилого віку. Мікрогеморагії відображають наявність відкладень гемосидерину, а їх Гістопатологічні корелятом є що відбулася раніше екстравазація крові. Вони можуть бути проявами геморагічної ангиопатии і вказувати на підвищену імовірність розвитку геморагічної трансформації на тлі антикоагулянтної, антитромботичної і тромболітичної терапії.Послідовності градієнтного відлуння, ЕПШ і ДВІ чутливі до паренхіматозним геморрагиям (первинне внутрішньомозковий крововилив і геморагічна трансформація) в надгострій фазі (перші кілька годин), в той час як рутинне МРТ в Т1-і Т2ВІ-режимах дозволяє виявляти крововиливу в підгострій і хронічній фазах. Послідовність FLAIR може виявитися корисною в діагностиці екстрааксіальних скупчень крові (субдуральна гематоми). Відповідно до вищевикладеного, в сучасних клінічних посібниках не рекомендується замінювати комп’ютерну томографію МРТ для відбору пацієнтів для проведення тромболізису.
ускладнення
Різні ускладнення можуть розвиватися у пацієнтів, у яких є металеві імплантати (перегрів, дисфункція водія ритму і т.п.). Тому необхідно пам’ятати про це і уточнювати МР-сумісність імплантатів у їх виробників. Якщо пацієнт страждає на клаустрофобію, то може застосовуватися легка седація або візуалізація за допомогою сканерів з відкритим контуром. Однак більшість таких апаратів дозволяють отримувати знімки більш низької якості. У рідкісних випадках відзначаються алергічні реакції на введення контрастної речовини для МРТ.
особливі міркування
Деяким пацієнтам (в критичному стані і тим, яким недавно був проведений тромболізис) застосування МРТ не цілком підходить, так як під час проведення дослідження немає можливості оцінки їх клінічного стану. Якщо МРТ все ж вкрай необхідна, то її проводять з мінімальним необхідним для встановлення діагнозу набором послідовностей, наприклад Т1, Т2, ДВІ або ПВІ і МР-ангіографія. У багатьох клініках розроблені спеціальні протоколи по ОІІ, спрямовані на мінімізацію тривалості обстеження. Пацієнтів, яким планується проведення МРТ, слід оцінювати на предмет наявності протипоказань, таких як клаустрофобія, металеві імплантати, водії ритму і МР-несумісні штучні серцеві клапани.